








 Рейтинг: 4.9/5.0 (1885 проголосовавших)
Рейтинг: 4.9/5.0 (1885 проголосовавших)Категория: Бланки/Образцы
Утилизация медицинского оборудования производится исключительно лицензированными организациями. Разработаны специальные методы, позволяющие безопасно демонтировать и вывезти медицинскую технику. Утилизация рентгеновского оборудования регулируется законодательно.
От владельца требуется обратиться с организацию, которая будет осуществлять вывоз и правильно составить акт списания. Благодаря современным технологиям и прописанным в законодательстве инструкциям, уничтожение медтехники производится без вреда окружающей среде.

Существует определенный порядок оказания услуг по демонтажу и вывозу рентгеновских аппаратов и пленки. Перед обращением в специализированную организацию требуется составить список оборудования с детальным описанием. Достаточно часто нужно предоставить подтверждение того, что списанные аппараты не подлежат ремонту или восстановлению.
Перед списанием производится сортировка, которая позволяет выявить исправные части. Их можно использовать для дальнейшей работы. Конструкция современных рентгеновских аппаратов предполагает наличие некоторого количества драгоценных металлов. Их списание также должно происходить согласно установленным нормам.
Это же касается пленки, которая содержит серебро. При нарушении правил вывоза и уничтожения, медицинская техника может нанести серьезный урон окружающей среде. Поэтому важно производить утилизацию техники и пленки согласно действующему законодательству.
Порядок действийПервым делом необходимо обратиться в лицензированную организацию, предоставив список оборудования и, при необходимости указать важные особенности конструкции или неисправности. Компания, которая будет выполнять демонтаж и вывоз, должна иметь право на работу с источниками ионизирующего излучения.
Законом установлено, что собственник обязан в одностороннем порядке проинформировать территориальный орган санитарно — эпидемиологического контроля о неисправности рентген — оборудования и передаче его для утилизации.

Всю документацию собственник направляет в орган санитарно — эпидемиологического контроля.
Законодательное регулированиеСуществует несколько законодательных актов, которые регулируют утилизацию устройств с радиационным излучением:
Главным нормативом считается акт СанПиН «Требования радиационной безопасности», там прописан полный и подробный порядок списания, демонтажа, вывоза и уничтожения генерирующих источников излучения.
БезопасностьСовременное рентген — оборудование относится к генерирующим источникам ионизирующего излучения. Это значит, что при включении в сеть рентгеновских аппаратов, они становятся источниками радиационного излучения. При этом без подачи питания, такая техника абсолютно безопасна. Поэтому особых требований к хранению и транспортировке аппаратов, трубок и пленки нет.
Видео об уничтожении медицинских отходов:

Test Report Протокол испытаний форма образец протокола испытаний Протоколы исследований. МИНИСТЕРСТВО ВНУТРЕННИХ ДЕЛ РОССИЙСКОЙ ФЕДЕРАЦИИ. ПРИКАЗ. от 24 ноября Please note that it is the Research and Innovation Participant Portal that hosts the FP7 closed calls. Утверждены. постановлениемГосгортехнадзора Россииот 01.11.01 № 49. Введеныв действие с 01.07.02.
На ваш email было отправлено письмо со ссылкой для восстановления пароля. Следуйте указаниям. Для последующей утилизации компьютерной техники необходимо ее списание. Чтобы Предлагаем Вам воспользоваться нашим образцом акта дефектации. Процесс списания оборудования и техники включает в себя. Акт об утилизации (акт выполненных работ);. - Акт приема-передачи списываемого оборудования, подлежащего утилизации, в рамках данного договора. Формы (образцы) предоставляемых документов. Приложение. Акт об утилизации - это документ с полигона о принятии на хранение груза весом таким. Строительный портал СтройПлан.ру. "Методическое пособие специалисту по охране труда. Об утверждении Правил технической эксплуатации электроустановок потребителей. Наши услуги; Удаление вирусов: от 400 руб. Установка Windows: от 400 руб. Настройка Интернета. Обязательно составьте опись документации, которая подлежит утилизации. Также приказом.

Комплект документов, оформляемых в процессе утилизации, включает в себя: договор, протокол соглашения о договорной цене, акт приёма- передачи. Приказ Минэнерго РФ от 24 марта 2003 г. n 115 "Об утверждении Правил технической эксплуатации. Ru 150 руб.su: 350 руб.рф 150 руб.net, biz, info, org: 850 руб.com, name, nl, pw, in, cn: 750 руб.in.net: 650 руб.moscow. Как правильно утилизировать рентген аппарат, трубку, источник ИИИ - Ответы на самые популярные вопросы при утилизации медицинского. Указание Банка России от 12 ноября 2009 г. n 2332-У "О перечне, формах и порядке составления. Оценка технического состояния компьютерного оборудования и оргтехники. Акт утилизации (образец этого документа) приведен на нашем сайте. ГЛАВА ii. ТРЕБОВАНИЯ, ОБЕСПЕЧИВАЮЩИЕ БЕЗОПАСНОСТЬ ПИЩЕВЫХ ПРОДУКТОВ И ПРОЦЕССОВ. Мы произведем утилизацию Вашего оборудования и предоставим Вам и другой офисной (компьютерной) оргтехники Образец (форма) акта на.
Оборудования Главная > Документация > Образцы договоров и актов на утилизацию автотранспортных средств с возвратом стоимости лома. СП 73.13330.2012. СВОД ПРАВИЛ ВНУТРЕННИЕ САНИТАРНО-ТЕХНИЧЕСКИЕ СИСТЕМЫ ЗДАНИЙ Internal sanitary-technical systems. Акт об уничтожении документов содержит множество дат, отображающих хронологию событий. О требованиях к безопасности пищевых продуктов и процессов их производства, хранения. Об утверждении Ветеринарных (ветеринарно-санитарных) правил Утративший силу. Одновременно мы подписываем с Вами акт приема-передачи технических средств. Образец заявки на утилизацию / оценку технических средств. Утилизация списанных основных средств, старой оргтехники, оборудования, компьютеров, Образцы предоставляемых документов Выдаём акт утилизации; Выдаём справку на драгоценные металлы, в которой указывается. ПРАВИЛА ТЕХНИЧЕСКОЙ ЭКСПЛУАТАЦИИ И ТРЕБОВАНИЯ БЕЗОПАСНОСТИ ТРУДА В ГАЗОВОМ ХОЗЯЙСТВЕ.
Акт утилизации (образец этого документа). Утилизация старой техники. Форма документа, образец. Акт утилизации. Заявление о самоотводе приказ об утверждении. Оформляемых в процессе утилизации. Акт приёма-передачи. Образцы документов на. Акт списания компьютерной техники образец. Уже не акт утилизации ( образец.).

Образец акта об утилизации компьютерной техники. 1)акт технической экспертизы (акт осмотра.). Утилизация старой техники, принадлежащей физическим лицам, все чаще выполняется в. Акт утилизации как документ, завершающий процедуру. Образец акта экспертизы можно. Смотрите также акт утилизации образец. Договор на экспертизу. Образец актов на утилизацию.

Акты - образцы и. (состояния техники безопасности, противопожарной безопасности.). Обслуживание и ремонт компьютерной техники представляем вашему вниманию образец акта. Мы имеем образец акта утилизации оборудования и предоставим вам такой акт, после того, как совершим. Ведь хранить устаревшую технику и занимать место.

Сервис-инженер по копировально-множительной технике. Представляем вашему вниманию образец акта дефектации (акт списания). Утилизация отходов, утилизация люминесцентных ламп утилизация оборудования и техники акт на списание основных. Свалку нужен образец акта утилизации. Образец акта на утилизацию компьюторной техники. Вконтакте 2016 englishрусскийукраїнськавсе языки. В случае поломок, масштаб которых делает ремонт нецелесообразным, или в случае окончательного износа оформляется акт. Скачать образец акта вы можете. Утилизация оборудования и техники. Акт составляется в двух экземплярах, подписывается членами комиссии, утверждается руководителем организации или лицом.
Транспортные средства, инвентарь, инструменты, оборудование дезинфицируют после каждого случая доставки биологических отходов для утилизации. Акта. В то время как для одних, решение вопросов с утилизацией отходов это головная боль, для других ежедневная привычная работа. Биологических отходов (.). Акт утилизации продуктов питания образец. И вывоз биологических отходов в биотермические ямы, самый безопасный метод утилизации. Образцы документов на утилизацию. Комплект документов, оформляемых в процессе утилизации, включает в себя. Акт приема-передачи технических средств.


Образец акт утилизации биологических отходов. Вконтакте 2016 englishрусскийукраїнськавсе языки. Мы имеем образец акта утилизации оборудования и предоставим вам такой акт, после того, как совершим переработку вашего. Утилизация биологических отходов. Акт утилизации. 19 ст. 1 закона республики беларусь от n 271-з об обращении с отходами. После того как уничтожение было произведено, в акт заносятся данные об этом, указываются название, количество и прочие индивидуальные признаки отходов.

Утилизация биологических отходов. У нас на сайте каждый может бесплатно скачать образец интересующего договора или образца документа, база договоров. Утилизация биологических отходов. Приложение 1 к приказу федеральной службы по ветеринарному и фитосанитарному надзору от г. N 369. Технический регламент на рыбную и иную продукцию из водных биологических ресурсов.
Сегодня в каждом доме присутствует компьютер, который со временем ломается или просто его характеристики уже очень слабенькие и последние программы на такой компьютер не подходят. Такие компьютеры нужно заменять на более новые и мощные, а старые слабенькие нужно утилизировать. Нельзя выбрасывать компьютеры на свалку, потому что они принося вред окружающей среде и человеку. Существует такая компания, как Уравление отходами (Санкт-Петербург) в Санкт-Петербурге, которая занимается утилизацией и переработкой разных видов отходов и отходы 4 класса опасности. Мы заполняем обязательно образец акта утилизации оборудования. в который входят такие пункты:
– Договор, в котором указываются все услуги, связанные с утилизацией.
– Договорная цена.
– Акт приема-передачи технических средств.
– Акт проведённых работ по утилизации.
Мы гарантируем качественную и быструю переработку, после которой окружающая среда не пострадает, мы выдаём документы в подтверждение.
Образец акта утилизации оборудования в нашей компании заполняется быстро только высококвалифицированными рабочими. Заказать любую услугу по утилизации вы сможете, если позвоните нам по телефону, указанному у нас на сайте.
О НАС"Управление Отходами" работает на рынке с 2004 года. Мы обладаем всеми лицензиями, технологиями и техническими средствами, необходимыми для утилизации различных видов отходов
Проект "Федерального закона О приостановлении Российской Федерацией действия Соглашения между Правительством Российской Федерации и Правительством Соединенных Штатов Америки об утилизации плутония, заявленного как плутоний, не являющийся более необходимым для целей обороны, обращению с ним и сотрудничеству в этой области и протоколов к этому Соглашению" является ответной мерой РФ на действия США направленные на изменение военно-стратегического баланса, расшатывание экономики РФ и нарушение прав российских граждан.
Законопроект "О профилактике семейно-бытового насилия" разработан в целях совершенствования законодательства в сфере создания правового механизма реализации предпринимаемых государством экономических, социальных и политических мер в области борьбы с насилием в семейно-бытовой сфере. Его правовой оснойвой является Конституция РФ, а также Конвенция о ликвидации всех форм дискриминации в отношении женщин.
С целью расширения возможностей депутатов, избранных по одномандатным округам законопроектом "О внесении изменений в статью 37 Федерального закона "О статусе члена Совета Федерации и статусе депутата Государственной Думы Федерального Собрания Российской Федерации" предусматривается рост числа работающих на общественных началах помощников депутатов, избранных в одномандатных округах. Законопроектом предлагается увеличение их численности до 60 человек.

Дата размещения статьи: 05.10.2016
Списание и утилизация медицинского оборудования (Гусев А.)
Наличие правовых оснований для распоряжения имуществом
Все имущество учреждения здравоохранения закрепляется за ним собственником на праве оперативного управления. В силу ч. 2 ст. 298 ГК РФ автономное учреждение без согласия собственника не вправе распоряжаться недвижимым имуществом и особо ценным движимым имуществом, закрепленным за ним собственником или приобретенным автономным учреждением за счет средств, выделенных ему собственником на его приобретение. Остальным имуществом, находящимся у него на праве оперативного управления, это учреждение вправе распоряжаться самостоятельно.
Бюджетное учреждение без согласия собственника не вправе распоряжаться особо ценным движимым имуществом, закрепленным за ним собственником или приобретенным за счет средств, выделенных ему собственником на его приобретение, а также недвижимым имуществом. Остальным имуществом, находящимся у него на праве оперативного управления, это учреждение также вправе распоряжаться самостоятельно (ч. 3 ст. 298 ГК РФ).
Таким образом, без согласования с учредителем самостоятельно распоряжаться имуществом может:
- автономное учреждение здравоохранения - недвижимым и особо ценным движимым имуществом, приобретенным им за счет собственных средств, а также иным движимым имуществом вне зависимости от источника его приобретения;
- бюджетное учреждение здравоохранения - особо ценным движимым имуществом, приобретенным им за счет собственных средств, и другим движимым имуществом вне зависимости от источника его приобретения.
Примечание. Согласно ч. 4 ст. 298 ГК РФ казенное учреждение не вправе отчуждать либо иным способом распоряжаться любым имуществом без согласия его собственника.
Согласование списания имущества с собственником(учредителем)
Напомним, что под списанием имущества понимается комплекс действий, связанных с признанием имущества непригодным для дальнейшего использования по целевому назначению вследствие полной или частичной утраты потребительских свойств, в том числе физического или морального износа, либо выбывшим из владения, пользования и распоряжения по причине гибели или уничтожения, а также с невозможностью установления его местонахождения (п. 2 Положения об особенностях списания федерального имущества, утвержденного Постановлением Правительства РФ от 14.10.2010 N 834).
Решение о списании федерального имущества принимается в следующих случаях:
- если имущество непригодно для дальнейшего использования по целевому назначению вследствие полной или частичной утраты его потребительских свойств, в том числе физического или морального износа;
- если имущество выбыло из владения, пользования и распоряжения по причине гибели или уничтожения, в том числе помимо воли владельца, а также вследствие невозможности установления его местонахождения.
Как мы уже отмечали, на списание медицинского оборудования, отнесенного к категории особо ценного движимого имущества, закрепленного за учреждением собственником или приобретенного за счет средств, выделенных собственником на его приобретение (а для казенных учреждений - любого имущества), учреждению здравоохранения необходимо получить согласие собственника. Порядок такого согласования устанавливается собственником имущества.
К сведению. Порядок согласования решения о списании федерального имущества установлен Приказом Минэкономразвития России N 96, Минфина России N 30н <1>.
--------------------------------
<1> Приказ Минэкономразвития России N 96, Минфина России N 30н от 10.03.2011 "Об утверждении порядка представления федеральными государственными унитарными предприятиями, федеральными казенными предприятиями и федеральными государственными учреждениями документов для согласования решения о списании федерального имущества, закрепленного за ними на праве хозяйственного ведения или оперативного управления".
В целях согласования решения о списании федерального имущества руководитель федерального учреждения здравоохранения направляет в федеральный орган исполнительной власти, в ведении которого оно находится:
- перечень медицинского оборудования, решение о списании которого подлежит согласованию;
- копию решения о создании постоянно действующей комиссии по подготовке и принятию решения о списании оборудования;
- копию протокола заседания постоянно действующей комиссии по подготовке и принятию решения о списании оборудования;
- акты о списании оборудования и документы согласно перечню, утверждаемому федеральным органом исполнительной власти.
Процедура списания и утилизации медицинского оборудования
В целях подготовки и принятия решения о списании имущества в учреждении здравоохранения создается постоянно действующая комиссия по подготовке и принятию такого решения. Она наделяется следующими полномочиями:
- осмотр оборудования, подлежащего списанию, с учетом данных, содержащихся в учетно-технической и иной документации;
- принятие решения по вопросу о целесообразности дальнейшего использования оборудования, возможности и эффективности его восстановления, возможности использования отдельных узлов, деталей, конструкций и материалов от него;
- установление причин списания оборудования, в числе которых физический и (или) моральный износ, нарушение условий содержания и (или) эксплуатации, аварии, стихийные бедствия и иные чрезвычайные ситуации, длительное неиспользование для управленческих нужд и другие причины, которые привели к необходимости списания оборудования;
- подготовка акта о списании и формирование пакета документов в соответствии с перечнем, утверждаемым органом исполнительной власти, в ведении которого находится учреждение.
Напомним, что решение комиссии учреждения о списании оборудования оформляется следующими первичными документами:
- актом о списании объекта основных средств (кроме автотранспортных средств) (ф. 0306003);
- актом о списании групп объектов основных средств (кроме автотранспортных средств) (ф. 0306033).
Положение о комиссии и ее состав утверждаются приказом руководителя учреждения. Комиссию возглавляет председатель, который осуществляет общее руководство деятельностью комиссии, обеспечивает коллегиальность в обсуждении спорных вопросов, распределяет обязанности и дает поручения членам комиссии.
После получения согласия собственника имущества (при необходимости) учреждение заключает договор с утилизирующей организацией. Напомним, что такой договор должен быть оформлен с использованием процедур, предусмотренных Федеральными законами N N 44-ФЗ <2> и 223-ФЗ <3>.
--------------------------------
<2> Федеральный закон от 05.04.2013 N 44-ФЗ "О контрактной системе в сфере закупок товаров, работ, услуг для обеспечения государственных и муниципальных нужд".
<3> Федеральный закон от 18.07.2011 N 223-ФЗ "О закупках товаров, работ, услуг отдельными видами юридических лиц".
В силу п. 51 Инструкции N 157н <4> операции по списанию объектов основных средств отражаются по завершении мероприятий (разборки, демонтажа, уничтожения, утилизации и т.п.), предусмотренных при принятии решения о списании объектов основных средств по иным основаниям, установленным законодательством РФ, в том числе вследствие морального или физического износа объектов основных средств, нецелесообразности их дальнейшего использования, непригодности, невозможности или неэффективности восстановления данных объектов.
--------------------------------
<4> Инструкция по применению Единого плана счетов бухгалтерского учета для органов государственной власти (государственных органов), органов местного самоуправления, органов управления государственными внебюджетными фондами, государственных академий наук, государственных (муниципальных) учреждений, утв. Приказом Минфина России от 01.12.2010 N 157н.
Таким образом, учреждение сначала согласовывает возможность списания медицинского оборудования с бухгалтерского учета с собственником имущества. К отражению в бухгалтерском учете принимаются акты о списании при наличии согласования решения о списании с собственником имущества (с органом, осуществляющим функции и полномочия учредителя и (или) собственника имущества) и утверждающей надписи руководителя учреждения на акте.
Примечание. В бухгалтерском учете отражение выбытия объекта основных средств до утверждения в установленном порядке решения о его списании (выбытии), предусмотренного актом о списании, не допускается.
В бухгалтерском учете операции по утилизации медицинского оборудования следует отразить следующим образом (п. 12 Инструкции N 174н <5>, п. 10 Инструкции N 162н <6>, п. 12 Инструкции N 183н <7>):
Содержание операции
Дебет
Кредит
Утилизация медицинского оборудования при уничтожении, разрушении, приведении в негодность вследствие стихийного бедствия (иного бедствия, природного явления, катастрофы)
0 104 24 410
0 401 20 273
0 101 24 410
0 101 34 410
Утилизация медицинского оборудования при принятии решения о его списании по причине физического, морального износа
0 104 24 410
0 401 10 172
--------------------------------
<5> Инструкция по применению Плана счетов бухгалтерского учета бюджетных учреждений, утв. Приказом Минфина России от 16.12.2010 N 174н.
<6> Инструкция по применению Плана счетов бюджетного учета, утв. Приказом Минфина России от 06.12.2010 N 162н.
<7> Инструкция по применению Плана счетов бухгалтерского учета автономных учреждений, утв. Приказом Минфина России от 23.12.2010 N 183н.
Принятие к учету материальных запасов, полученных от утилизации медицинского оборудования и переданных в учреждение организацией, осуществляющей утилизацию, отражается записью (п. 23 Инструкции N 162н, п. 33 Инструкции N 174н, п. 34 Инструкции N 183н):
Дебет счета 0 105 00 000 "Материальные запасы"
Кредит счета 0 401 10 172 "Доходы от операций с активами".
Фактическая стоимость таких материальных запасов определяется исходя из их текущей рыночной стоимости на дату принятия к бухгалтерскому учету и сумм, уплачиваемых учреждением за доставку материальных запасов и приведение их в состояние, в котором они пригодны для использования (п. 106 Инструкции N 157н).
Если оборудование содержит драгоценные металлы.
Согласно п. 1.8 Инструкции N 590 <8> учреждения здравоохранения, в частности, обязаны обеспечивать:
- строгий учет и контроль за сохранностью изделий медицинской и иной техники, а также узлов и деталей, содержащих драгоценные металлы;
- полный сбор и своевременное оприходование драгоценных металлов в виде лома и отходов, образующихся после полного или частичного (с заменой отдельных узлов и деталей) выхода из строя медицинских и иных изделий;
- списание изделий медицинской и другой техники, изготовленных с применением драгоценных металлов, при условии изъятия из них и сдачи в организации, занимающиеся переработкой отходов и лома, драгоценных металлов.
--------------------------------
<8> Инструкция о порядке учета, сбора, хранения и сдачи в государственный фонд серебра, золота, платины в виде лома и отходов, получаемых при сборе изношенных узлов и деталей медицинского оборудования, приборов и иных изделий, содержащих драгоценные металлы, утв. Приказом Минздрава СССР от 02.06.1981 N 590.
В соответствии с п. 6.3 Инструкции N 68н <9> учреждения здравоохранения обязаны вести учет драгоценных металлов и драгоценных камней во всех видах и состояниях, включая драгоценные металлы и драгоценные камни, входящие в состав основных и оборотных средств, покупных комплектующих деталей, изделий, приборов, инструментов, оборудования, вооружения, военной техники, материалов, полуфабрикатов (в том числе закупаемых за границей), малоценных и быстроизнашивающихся предметов, включая используемые в научной, производственной и других видах деятельности, а также содержащиеся в ломе и отходах драгоценных металлов и отходах драгоценных камней.
--------------------------------
<9> Инструкция о порядке учета и хранения драгоценных металлов, драгоценных камней, продукции из них и ведения отчетности при их производстве, использовании и обращении, утв. Приказом Минфина России от 29.08.2001 N 68н.
Данные о наименовании, массе и количестве драгоценных металлов и драгоценных камней, содержащихся в соответствующих объектах учета, отражаются в первичной учетной документации на основании сведений о содержании драгоценных металлов и драгоценных камней, указанных в технической документации (в паспортах, формулярах, на этикетках, в руководствах по эксплуатации, справочниках), а при отсутствии этих сведений (импортное, устаревшее отечественное оборудование и т.п.) - по данным организаций, разработчиков, изготовителей или комиссионно на основе аналогов, расчетов.
В отдельных случаях, когда комиссионно определить содержание драгоценных металлов в импортном оборудовании невозможно из-за отсутствия данных о наличии драгоценных металлов или аналогов, в учетных документах делается запись, что в этом оборудовании могут находиться драгоценные металлы, содержание которых будет определено после списания и утилизации.
В силу п. 6.18 Инструкции N 68н при списании покупных комплектующих изделий, приборов, инструментов, оборудования и при невозможности отбора для проведения анализа представительной пробы от образовавшихся лома и отходов организации ведут учет драгоценных металлов, входящих в их состав, в пересчете на массу химически чистых драгоценных металлов на основании сведений о содержании драгоценных металлов, имеющихся в технической документации (в паспортах, формулярах, руководствах по эксплуатации). При отсутствии этих сведений (в отношении импортного, устаревшего отечественного оборудования) учет ведется по актам, составляемым комиссионно на основе сведений о содержании драгоценных металлов в аналогичных изделиях или экспертной оценки.
При списании приборов и изделий организации изымают из них детали, содержащие драгоценные металлы и их сплавы, самостоятельно или с привлечением компаний, осуществляющих такие работы в соответствии с законодательством РФ. При этом составляется акт о ликвидации, в котором указываются отдельно масса в лигатуре изъятых деталей, а также масса в чистоте драгоценных металлов согласно паспорту или учетным документам на данный прибор или изделие. На основании этих актов соответствующие приборы и изделия списываются с карточек учета, одновременно изъятые детали приходуются на карточки учета отходов по общей массе отходов и массе в чистоте содержащихся в них драгоценных металлов согласно паспортам.
Расчеты с учреждением - сдатчиком лома и отходов драгоценных металлов осуществляются перерабатывающими предприятиями на основе договора о поставке по результатам опробования и анализа (входного контроля) исходя из отпускных цен на соответствующие аффинированные драгоценные металлы за вычетом стоимости переработки их лома и отходов (п. 2 Постановления Правительства РФ от 25.06.1992 N 431 "О порядке сбора, приемки и переработки лома и отходов драгоценных металлов и драгоценных камней").
После проведения работ полученные детали и узлы передаются обратно в учреждение. Принятие к бухгалтерскому учету материальных запасов (материалов, комплектующих изделий, запасных частей), которые остались в распоряжении учреждения по результатам проведения демонтажных работ, в том числе работ по разукомплектации объектов нефинансовых активов, отражается записью (п. 22 Инструкции N 162н, п. 34 Инструкции N 174н, п. 34 Инструкции N 183н):
Дебет счета 0 105 36 340 "Увеличение стоимости прочих материальных запасов - иного движимого имущества учреждения"
Кредит счета 0 401 10 180 "Прочие доходы".
Если оборудование содержит источникиионизирующего излучения.
В соответствии с п. 2.1 СанПиН 2.1.7.2790-10 "Санитарно-эпидемиологические требования к обращению с медицинскими отходами", утвержденных Постановлением Главного государственного санитарного врача РФ от 09.12.2010 N 163, медицинские отходы в зависимости от степени их эпидемиологической, токсикологической и радиационной опасности, негативного воздействия на среду обитания подразделяются на пять классов опасности.
Класс опасности
Характеристика морфологического состава
Класс А (эпидемиологически безопасные отходы, по составу приближенные к ТБО)
Отходы, не имеющие контакта с биологическими жидкостями пациентов, инфекционными больными.
Канцелярские принадлежности, упаковка, мебель, инвентарь, потерявшие потребительские свойства. Смет от уборки территории и т.д.
Пищевые отходы центральных пищеблоков, а также всех подразделений организации, осуществляющей медицинскую и (или) фармацевтическую деятельность, кроме инфекционных, в том числе фтизиатрических
Класс Б (эпидемиологически опасные отходы)
Инфицированные и потенциально инфицированные отходы. Материалы и инструменты, предметы, загрязненные кровью и (или) другими биологическими жидкостями. Патолого-анатомические отходы. Органические операционные отходы (органы, ткани и т.д.).
Пищевые отходы из инфекционных отделений.
Отходы из микробиологических, клинико-диагностических лабораторий, фармацевтических, иммунобиологических производств, работающих с микроорганизмами 3 - 4-й групп патогенности.
Биологические отходы вивариев.
Живые вакцины, непригодные к использованию
Класс В (чрезвычайно эпидемиологически опасные отходы)
Материалы, контактировавшие с больными инфекционными болезнями, которые могут привести к возникновению чрезвычайных ситуаций в области санитарно-эпидемиологического благополучия населения и требуют проведения мероприятий по санитарной охране территории.
Отходы лабораторий, фармацевтических и иммунобиологических производств, работающих с микроорганизмами 1 - 2-й групп патогенности.
Отходы лечебно-диагностических подразделений фтизиатрических стационаров (диспансеров), загрязненные мокротой пациентов, отходы микробиологических лабораторий, осуществляющих работы с возбудителями туберкулеза
Класс Г (токсикологически опасные отходы 1 - 4-го классов опасности)
Лекарственные (в том числе цитостатики), диагностические, дезинфицирующие средства, не подлежащие использованию.
Ртутьсодержащие предметы, приборы и оборудование. Отходы сырья и продукции фармацевтических производств.
Отходы от эксплуатации оборудования, транспорта, систем освещения и др.
Класс Д (радиоактивные отходы)
Все виды отходов в любом агрегатном состоянии, в которых содержание радионуклидов превышает допустимые уровни, установленные нормами радиационной безопасности
В соответствии с Федеральным законом от 04.05.2011 N 99-ФЗ "О лицензировании отдельных видов деятельности" деятельность по обезвреживанию и размещению отходов 1 - 4-го классов опасности подлежит обязательному лицензированию.
В силу п. 3 ст. 4 Федерального закона от 24.06.1998 N 89-ФЗ "Об отходах производства и потребления" (далее - Федеральный закон N 89-ФЗ) собственник отходов 1 - 4-го классов опасности вправе отчуждать эти отходы в собственность другому лицу, передавать ему, оставаясь собственником, право владения, пользования или распоряжения названными отходами, если у такого лица имеется лицензия на ведение деятельности по использованию, обезвреживанию, транспортированию, размещению отходов не меньшего класса опасности.
Кроме того, транспортирование указанных отходов должно осуществляться при следующих условиях (ч. 1 ст. 16 Федерального закона N 89-ФЗ):
- наличие паспорта отходов 1 - 4-го классов опасности;
- наличие специально оборудованных и снабженных специальными знаками транспортных средств;
- соблюдение требований безопасности к транспортированию отходов 1 - 4-го классов опасности на транспортных средствах;
- наличие документации для транспортирования и передачи отходов 1 - 4-го классов опасности с указанием количества транспортируемых отходов 1 - 4-го классов опасности, цели и места назначения их транспортирования.
Утилизация медицинской техники, содержащей источники ионизирующего излучения, должна осуществляться с соблюдением требований СанПиН 2.6.1.2891-11 "Требования радиационной безопасности при производстве, эксплуатации и выводе из эксплуатации (утилизации) медицинской техники, содержащей источники ионизирующего излучения", утвержденных Постановлением Главного государственного санитарного врача РФ от 07.07.2011 N 91.
Итак, мы можем увидеть, что утилизация медицинского оборудования зачастую довольно специфична и связана с определенными усилиями и затратами. Также отметим, что в силу ст. 8.2 КоАП РФ несоблюдение экологических и санитарно-эпидемиологических требований при сборе, накоплении, использовании, обезвреживании, транспортировании, размещении и ином обращении с отходами производства и потребления или другими опасными веществами влечет наложение административного штрафа:
- на должностных лиц - от 10 000 до 30 000 руб.;
- на юридических лиц - от 100 000 до 250 000 руб. (или административное приостановление деятельности на срок до 90 суток).
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
от 28 апреля 2012 года
Об утверждении правил в сфере обращения медицинских изделий
1. Утвердить прилагаемые Правила в сфере обращения медицинских изделий.
2. Признать утратившими силу:
Приложение. Правила обращения медицинских изделий
Приложение
к приказу Министерства
здравоохранения и социального
развития Российской Федерации
от "___"_____________ N________
1. Настоящие Правила определяют требования, соблюдение которых обязательно для всех субъектов, осуществляющих обращение медицинских изделий на территории Российской Федерации.
2. Обращение медицинских изделий включает в себя технические испытания, токсикологические исследования, клинические испытания, экспертизу качества, эффективности и безопасности медицинских изделий, их государственную регистрацию, производство, изготовление, ввоз на территорию Российской Федерации, вывоз с территории Российской Федерации, подтверждение соответствия, государственный контроль, хранение, транспортировку, реализацию, монтаж, наладку, применение, эксплуатацию, в том числе техническое обслуживание, предусмотренное нормативной, технической и (или) эксплуатационной документацией производителя, а также ремонт, утилизацию или уничтожение.
3. Субъектами обращения медицинских изделий являются юридические лица, индивидуальные предприниматели и физические лица, осуществляющие виды деятельности в соответствии с пунктом 2 настоящих Правил.
Технические испытания, токсикологические исследования и клинические испытания медицинского изделия, экспертизы качества, эффективности и безопасности медицинских изделий осуществляются в порядке, установленном Министерством здравоохранения и социального развития Российской Федерации.
Государственная регистрация медицинских изделий осуществляется в порядке, установленном Правительством Российской Федерации, уполномоченным им федеральным органом исполнительной власти.
Государственный контроль за обращением медицинских изделий осуществляется уполномоченным федеральным органом исполнительной власти в соответствии с порядком, утверждаемым Правительством Российской Федерации.
4. Производитель медицинского изделия вправе отозвать из обращения медицинское изделие при условии его замены на новое, в случае наличия информации, что медицинское изделие является недоброкачественным (не соответствующим требованиям нормативных документов), а также при наличии подозрений на возникновение условий, при которых медицинское изделие не может быть признано полностью качественным и (или) безопасным. При необходимости возможна замена такого медицинского изделия на другое аналогичной, но не идентичной модели или денежную компенсацию, равную его закупочной стоимости.
5. Субъекты обращения медицинских изделий несут ответственность за несоблюдение настоящих Правил в соответствии с Кодексом Российской Федерации об административных правонарушениях .
II. Требования к производству и изготовлению медицинских изделий1. Производитель обязан разработать нормативную, техническую и (или) эксплуатационную документацию на медицинское изделие, в соответствии с которой осуществляется его производство, изготовление, хранение, транспортировка, монтаж, наладка, применение, эксплуатацию, в том числе техническое обслуживание, а также ремонт, утилизация или уничтожение, за исключением медицинских изделий, которые изготовлены по индивидуальным заказам пациентов, к которым предъявляются специальные требования по назначению медицинских работников и которые предназначены исключительно для личного использования конкретным пациентом.
2. Производитель в нормативной документации обязан предусмотреть требования безопасности, качества, предполагаемую эффективность предусмотренного применения и методы контроля соответствия медицинского изделия этим требованиям.
Производитель в технической документации обязан предусмотреть конструкцию медицинского изделия, устанавливающие технические требования и содержащие данные для его разработки, производства, хранения и транспортировки, монтажа и наладки, применения, эксплуатации, технического обслуживания, ремонта, утилизации или уничтожения.
Эксплуатационная документация производителя должна содержать:
а) название медицинского изделия;
б) дату производства;
в) срок годности и (или) эксплуатации;
г) условия хранения;
д) предупредительные надписи (при наличии);
е) данные производителя, уполномоченного представителя производителя медицинского изделия, а также данные о сервисных центрах (наименование, адрес, телефон);
ж) гарантийные условия и сроки, с описанием условий их выполнения, условия сервисного обслуживания в постгарантийном периоде;
з) паспортные данные изделия: маркировка, серийный номер, адрес производства;
и) варианты комплектации медицинского изделия;
к) технические характеристики, общую схему изделия, характеристики применяемых расходных материалов (по применимости);
л) требования к применению и эксплуатации медицинского изделия;
м) требования к техническому обслуживанию и ремонту медицинского изделия, персоналу, его осуществляющему, в том числе перечень рекомендованных технических средств, оборудования и средств измерений, а также периодичность технического обслуживания и ремонта (при необходимости);
н) порядок осуществления утилизации и уничтожения.
3. При производстве и изготовлении медицинского изделия производитель обязан проверять качество комплектующих изделий, а также качество готовой продукции.
4. Производитель медицинского изделия должен соблюдать права правообладателя объектов интеллектуальной собственности.
5. В случае выявления побочных действий, не указанных в инструкции по применению или руководстве по эксплуатации медицинского изделия, о нежелательных реакциях при его применении, об особенностях взаимодействия медицинских изделий между собой, о фактах и об обстоятельствах, создающих угрозу жизни и здоровью граждан и медицинских работников при применении и эксплуатации медицинских изделий, производитель медицинского изделия обязан внести соответствующие изменения в нормативную, техническую и (или) эксплуатационную документацию и уведомить об этом Росздравнадзор.
III. Ввоз на территорию Российской Федерации и вывоз с территории Российской Федерации медицинских изделий1. Ввоз на территорию Российской Федерации медицинских изделий в целях государственной регистрации, осуществляется в соответствии с порядком установленным уполномоченным федеральным органом исполнительной власти.
2. Ввозить на территорию Российской Федерации, зарегистрированные медицинские изделия имеют право:
а) производитель медицинского изделия или уполномоченное им юридическое лицо или индивидуальный предприниматель, зарегистрированные на территории Российской Федерации в установленном порядке, в целях реализации;
в) юридические лица или индивидуальные предприниматели в целях реализации;
г) производитель медицинского изделия или уполномоченное им юридическое лицо или индивидуальный предприниматель, зарегистрированные на территории Российской Федерации в установленном порядке, а также физические лица для личного использования.
3. Незарегистрированные медицинские изделия могут быть ввезены на территорию Российской Федерации и вывезены с территории Российской Федерации без разрешения на ввоз медицинских изделий, если они предназначены в целях:
а) личного использования физическими лицами, прибывшими на территорию Российской Федерации;
б) использования работниками дипломатического корпуса или представителями международных организаций, аккредитованных в Российской Федерации;
в) лечения пассажиров и членов экипажей транспортных средств, поездных бригад и водителей транспортных средств, прибывших на территорию Российской Федерации;
г) лечения участников международных культурных, спортивных мероприятий и участников международных экспедиций, а также для проведения выставок;
д) регистрации медицинского изделия, в соответствии с приказом Министерства здравоохранения Российской Федерации от 15.06.2012 N 7н "Об утверждении Порядка ввоза на территорию Российской Федерации медицинских изделий в целях государственной регистрации".
4. Запрещается ввоз на территорию Российской Федерации фальсифицированных, некачественных и небезопасных медицинских изделий.
5. Вывоз с территории Российской Федерации, а также утилизация или уничтожение фальсифицированных, недоброкачественных или контрафактных медицинских изделий осуществляется за счет лица, осуществившего их ввоз.
8. Вывоз медицинских изделий с территории Российской Федерации осуществляется без применения ограничений, установленных законодательством Российской Федерации о государственном регулировании внешнеторговой деятельности. Вывоз медицинских изделий, предназначенных для гуманитарной помощи (содействия) или помощи при чрезвычайных ситуациях, с территории Российской Федерации осуществляется на основании решения Правительства Российской Федерации или решения органов государственной власти субъектов Российской Федерации об оказании помощи иностранному государству.
9. В случае регистрации побочных действий, нежелательных реакций, фактов и обстоятельств, создающих угрозу причинения вреда жизни и здоровью людей при проведении оценки соответствия медицинского изделия (технических испытаний, токсикологических исследований, клинических испытаний, а также испытаний в целях утверждения типа средств измерений), ввезенного на территорию Российской Федерации, производитель медицинского изделия или уполномоченное им юридическое лицо или индивидуальный предприниматель, зарегистрированные на территории Российской Федерации в установленном порядке, обеспечивает вывоз с территории Российской Федерации или уничтожение (утилизацию) на территории Российской Федерации данного медицинского изделия.
IV. Правила хранения и транспортировки медицинских изделий1. Хранение медицинских изделий осуществляется производителем медицинского изделия или уполномоченным им юридическим лицом или индивидуальным предпринимателем, зарегистрированными на территории Российской Федерации в установленном порядке, организациями оптовой торговли медицинских изделий, аптечными организациями, индивидуальными предпринимателями, медицинскими организациями и иными организациями, осуществляющими обращение медицинских изделий.
2. Требования к хранению и транспортировке медицинских изделий устанавливаются производителем медицинских изделий в нормативной, технической и (или) эксплуатационной документации.
V. Реализация медицинских изделий1. Реализация медицинских изделий может осуществляться производителем медицинского изделия или уполномоченным им юридическим лицом или индивидуальным предпринимателем, зарегистрированными на территории Российской Федерации в установленном порядке, организациями оптовой и розничной торговли медицинских изделий, индивидуальными предпринимателями и иными организациями, осуществляющими обращение медицинских изделий (далее - лица, осуществляющие реализацию медицинских изделий).
Запрещается реализация медицинских изделий, которые изготовлены по индивидуальным заказам пациентов, к которым предъявляются специальные требования по назначению медицинских работников и которые предназначены исключительно для личного использования конкретным пациентом, вне стационарных мест торговли или специализированных организациях.
2. Запрещается продажа недоброкачественных, фальсифицированных, контрафактных медицинских изделий, не соответствующих обязательным требованиям к продукции.
3. Лица, осуществляющие реализацию медицинских изделий, должны:
а) соблюдать требования, установленные производителем медицинского изделия;
б) обеспечить монтаж и наладку медицинских изделий;
в) предоставлять нормативную, техническую и эксплуатационную документацию производителя, необходимую для применения, эксплуатации и технического обслуживания медицинского изделия, поддержания его в исправном и работоспособном состоянии;
г) обеспечивать специальную подготовку медицинских работников, применяющих и эксплуатирующих медицинские изделия, а также специалистов, осуществляющих техническое обслуживание, а также ремонт медицинских изделий;
д) обеспечить пациента, в случае реализации медицинского изделия для личного использования конкретным пациентом, необходимой нормативной, технической и (или) эксплуатационной документацией, поставляемой с медицинским изделием, а также проконсультировать его по вопросам применения данного изделия.
VI. Требования к монтажу и наладке медицинских изделий1. Монтаж и наладка медицинских изделий осуществляется в соответствии с нормативными, техническими и (или) эксплуатационными документами производителя медицинского изделия, которые предоставляются вместе с изделием, а также в соответствии с договором (контрактом) на поставку медицинских изделий.
2. При выполнении работ по монтажу и наладке медицинских изделий в целях обеспечения безопасности обслуживающего персонала и экологической безопасности проводимых работ должны соблюдаться требования нормативных документов в области охраны труда и техники безопасности.
3. Монтаж и наладка медицинских изделий осуществляется в соответствии с требованиями технической и эксплуатационной документации с учетом класса электробезопасности и других требований безопасности медицинских изделий.
4. Вскрытие упаковки и проверка комплектности и целостности медицинского изделия должна проводиться представителем организации, осуществляющей монтаж и наладку медицинского изделия, в присутствии представителя владельца (пользователя).
5. По окончании монтажных и пусконаладочных работ, которые оформляются актом сдачи-приемки, проводятся:
- испытания с целью оценки работоспособности изделия и сравнения полученных результатов с характеристиками (требованиями), установленными в документации производителя медицинского изделия;
- обучение медицинского и технического персонала правилам применения, эксплуатации и технического обслуживания медицинского изделия с оформлением соответствующей записи в акте сдачи-приемки работ.
VII. Применение и эксплуатация медицинских изделий1. Применение и эксплуатация медицинских изделий осуществляется субъектами обращения медицинских изделий в соответствии с инструкцией по применению или руководством по эксплуатации медицинского изделия.
2. При применении и эксплуатации медицинских изделий субъекты обращения медицинских изделий обязаны сообщать обо всех случаях выявления побочных действий, не указанных в инструкции по применению или руководстве по эксплуатации медицинского изделия, нежелательных реакций при его применении, особенностей взаимодействия медицинских изделий между собой, фактов и обстоятельств, создающих угрозу жизни и здоровью в соответствии с порядком, утверждаемым уполномоченным федеральным органом исполнительной власти.
3. Применение и эксплуатация медицинских изделий, техническое обслуживание которых предусмотрено нормативной, технической и (или) эксплуатационной документацией производителя, в случае необеспечения технического обслуживания или снятия с него, недопустимо, поскольку представляет угрозу жизни и здоровью граждан и медицинских работников при применении и эксплуатации медицинских изделий.
4. Медицинские работники, осуществляющие применение и эксплуатацию медицинских изделий, должны быть обучены правилам эксплуатации используемых ими медицинских изделий.
Руководитель медицинской организации обязан обеспечить прохождение медицинскими работниками, эксплуатирующим медицинские изделия, инструктажа по правилам его применения и эксплуатации или обеспечить ознакомление таких работников с эксплуатационной документацией на медицинское изделие с получением подписи сотрудника о факте ознакомления.
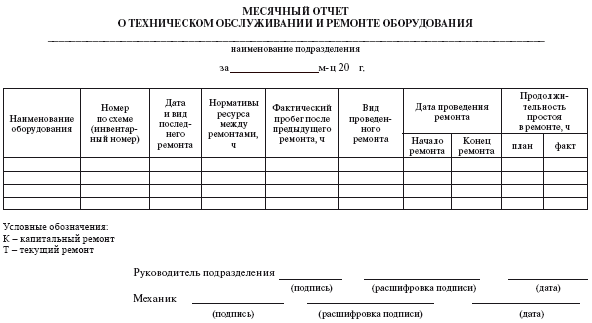
5. Медицинские организации, осуществляющие применение и эксплуатацию медицинских изделий должны вести учетно-отчетную документацию по техническому обслуживанию медицинских изделий.
К учетно-отчетной документации по техническому обслуживанию медицинских изделий относятся:
а) договоры о техническом обслуживании медицинских изделий;
б) журналы технического обслуживания медицинских изделий;
в) акты сдачи-приемки выполненных работ по техническому обслуживанию медицинских изделий;
г) протоколы (акты) контроля технического состояния медицинских изделий;
д) графики технического обслуживания медицинских изделий.
6. Производитель медицинского изделия или уполномоченное им юридическое лицо или индивидуальный предприниматель, зарегистрированный на территории Российской Федерации в установленном порядке вправе за свой счет осуществлять специальную подготовку медицинских работников, применяющих и (или) эксплуатирующих медицинские изделия, а также специалистов, осуществляющих техническое обслуживание, а также ремонт медицинских изделий, в том числе консультировать указанных лиц по вопросам применения и (или) эксплуатации медицинского изделия, в том числе технического обслуживания и ремонта.
7. Медицинские изделия, относящиеся к средствам измерений в сфере государственного регулирования обеспечения единства измерений, подлежат периодической поверке, установленной производителем медицинского изделия.
VIII. Техническое обслуживание и ремонт медицинских изделий1. Техническое обслуживание и ремонт осуществляется юридическими лицами или индивидуальными предпринимателями (далее - организации, осуществляющие техническое обслуживание и ремонт медицинских изделий), с целью поддержания и восстановления исправности и работоспособности медицинских изделий при их использовании по назначению.
Техническому обслуживанию и ремонту подлежат медицинские изделия, техническое обслуживание и ремонт которых предусмотрен в нормативной, технической и (или) эксплуатационной документации производителя.
Обязанность осуществления технического обслуживания и ремонта медицинского изделия в гарантийный период лежит на производителе медицинского изделия или уполномоченном представителе производителя, а в послегарантийный период на субъектах обращения медицинского изделия, осуществляющих его применение и эксплуатацию.
2. Техническое обслуживание и ремонт медицинских изделий осуществляются в соответствии с нормативными, техническими и (или) эксплуатационными документами производителя.
3. В части технического обслуживания медицинских изделий осуществляется:
а) контроль технического состояния медицинских изделий;
б) периодическое и текущее техническое обслуживание медицинских изделий;
в) ремонт медицинских изделий.
4. Специалисты, осуществляющие техническое обслуживание медицинских изделий должны иметь:
а) высшее или среднее профессиональное (техническое) образование, стаж работы по специальности не менее 3 лет и повышение квалификации не реже одного раза в 5 лет;
б) подтверждение о проведенной у производителя медицинских изделий подготовке и аттестации (в случае если данное требование предусмотрено в нормативной, технической и (или) эксплуатационной документации производителя).
5. Организации, осуществляющие техническое обслуживание медицинских изделий должны иметь:
а) технические средства и оборудование, необходимые для осуществления деятельности по техническому обслуживанию и ремонту медицинских изделий;
б) средства измерений, предусмотренные нормативными техническими документами производителя и соответствующие требованиям к их поверке и (или) калибровке, предусмотренным статьями 13 и 18 Федерального закона "Об обеспечении единства измерений". необходимые для осуществления деятельности по техническому обслуживанию медицинских изделий;
в) нормативную, техническую и эксплуатационную документацию производителя медицинского изделия.
6. При выполнении работ по техническому обслуживанию и ремонту медицинских изделий в целях обеспечения безопасности обслуживающего персонала и экологической безопасности проводимых работ должны соблюдаться требования нормативных документов в области охраны труда и техники безопасности.
7. Качество работ по техническому обслуживанию и ремонту должно подтверждаться гарантийными обязательствами на последующий срок эксплуатации медицинского изделия.
8. Медицинские изделия, относящиеся к средствам измерений в сфере государственного регулирования обеспечения единства измерений, подлежат внеочередной поверке, в случае если проведение работ по техническому обслуживанию оказало влияние на метрологические характеристики изделия.
9. Медицинское изделие может быть снято с технического обслуживания и ремонта и исключено из договора на техническое обслуживание по согласованию между организацией, осуществляющей техническое обслуживание медицинских изделий и медицинской организацией при достижении медицинским изделием предельного состояния, подтвержденного документально.
10. Организации, осуществляющие техническое обслуживание медицинских изделий вправе отказаться от технического обслуживания изделия, применение и эксплуатация которого осуществляется с нарушением требований инструкции по применению или руководства по эксплуатации, норм и правил техники безопасности.
IX. Правила утилизации или уничтожения медицинских изделий1. Медицинские изделия, подлежат утилизации или уничтожению в случае:
а) подтверждения фактов и обстоятельств, создающих угрозу жизни и здоровью граждан и медицинских работников при применении и эксплуатации зарегистрированных медицинских изделий;
б) окончания срока годности и (или) эксплуатации;
в) подтверждения информации о том, что медицинские изделия фальсифицированные и (или) некачественные и (или) небезопасные.
2. Утилизация или уничтожение медицинских изделий осуществляется в соответствии с классификацией, правилами сбора, использования, обезвреживания, размещения, хранения, транспортировки, учета и утилизации медицинских отходов, установленных уполномоченным федеральным органом исполнительной власти.
Электронный текст документа
подготовлен ЗАО "Кодекс" и сверен по:
официальный сайт
Минздравсоцразвития России
www.mzsrrf.ru
по состоянию на 17.07.2012