


 Рейтинг: 4.2/5.0 (1934 проголосовавших)
Рейтинг: 4.2/5.0 (1934 проголосовавших)Категория: Инструкции
Гемоглобин окисляют в метгемоглобин (гемиглобин) железосинеродистым калием (красная кровяная соль); образующийся с ацетонциангидрином окрашенный цианметгемоглобин (гемиглобинцианид) определяют колориметрически.
Фотоэлектроколориметр (ФЭК-56М или другой).
В пробирку к 5 мл трансформирующего раствора добавляют 0,02 мл крови (разведение в 251 раз). Содержимое пробирки тщательно перемешивают и оставляют стоять на 10 мин. Измеряют на фото-электроколориметре при длине волны 500— 560 нм (зеленый светофильтр) в кювете с толщиной слоя 1 см против холостой пробы (трансформирующий раствор). Измеряют при тех же условиях стандартный раствор.
Расчет содержания гемоглобина производят по калибровочному графику (см. ниже), построенному по стандартному раствору гемиглобинцианида, или по формуле:
где ЕОП — экстинкция опытной пробы; ЕСТ — экстинкция стандартного раствора; С— концентрация гемиглобинцианида в стандартном растворе, мг%; К — коэффициент разведения крови; 0,001 — коэффициент для пересчета мг/100 мл в г/100 мл.
Стандартный раствор, мл
Трансформирующий раствор, мл
- цианметгемоглобиновый метод Драбкина ( гемиглобинцианидный метод)
- гемиглобиновый метод (гемихромный метод)
Гемиглобинцианидный метод (метод Драбкина)
рекомендован Международным комитетом по стандартизации в гематологии в качестве референтного. В этом методе Fe ² гемоглобина окисляется до Fe ³ метгемоглобина. Метгемоглобин переводится в стабильный цианметгемоглобин цианидом.
Гемиглобинцианидный метод характеризуется высокой точностью, простотой исполнения, дешевизной и возможностью выполнения на гематологических анализаторах.
В настоящее время многие фирмы выпускают наборы реактивов для определения концентрации гемоглобина. Используя в качестве калибратора растворы гемиглобинцианида разной концентрации (НПО «Ренам», ЗАО «Медлакор», «Лахема» и др). Точные значения концентрации гемиглобинцианида и гемоглобина для каждой серии указаны в паспорте набора.
зарегистрирован МЗ РФ и рекомендован для применения в КДЛ.
В отличие от гемиглобинцианидного метода не проводится перевод метгемоглобина в цианметгемоглобин, поэтому не используются цианистые соединения. Максимум поглощения гемихрома находится на длине волны 533 нм. Однако измерение на этой длине волны возможно только в спектрофотометрических приборах, где можно установить любую длину волны.
На фотометрах используется длина волны в 540 нм, что в данном случае не совсем корректно.
Аммиачный метод (модифицированный метод Дервиза-Воробьева)
Метод также рекомендован МЗ РФ для использования в практике КДЛ.
Сущность метода заключается в том, что все разновидности гемоглобина не переводятся в единую форму, а выполняется разведение пробы крови в 0,04% растворе аммиака.
Этот метод реализован в гемоглобинометре «МиниГЕМ-523».
Факторы, влияющие на величину гемоглобина:
- Скорость синтеза гемоглобина в эритрокариоцитах
- Объем плазмы (гоповолемия. гиперволемия)
Факторы, приводящие к ложно завышенным значениям гемоглобина:
- WBC > 100х109/л,
- наличие HbC или HbS,
- наличие легкопреципитирующих глобулинов (миеломная б-нь, б-нь Вальденстрема)
Значение параметров ОАК больного с ХМЛ с гиперлипидемией, полученные на двух анализаторах
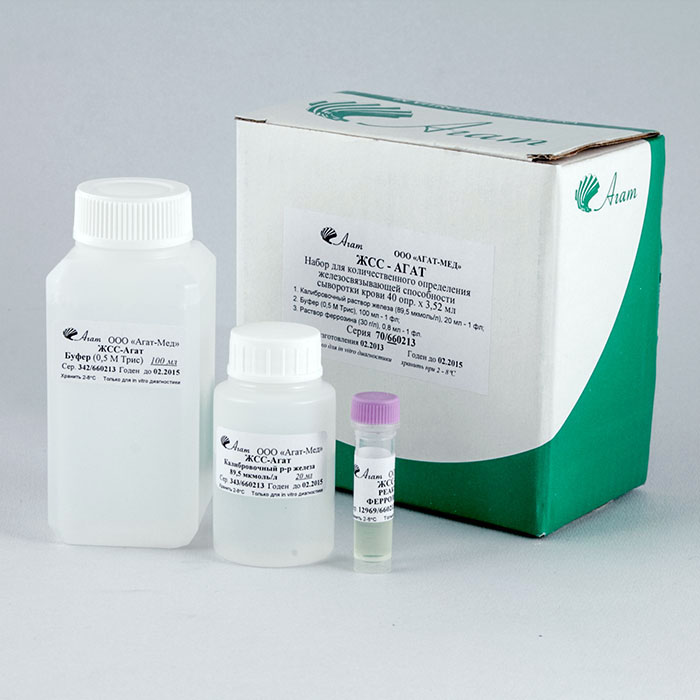
Набор предназначен для количественного определения содержания гемоглобина в крови гемиглобинцианидным методом (метод Drabkin) в клинико-диагностических и биохимических лабораториях.
Набор рассчитан на проведение 600 определений при расходе 5,0 мл рабочего раствора на один анализ.
НАЗНАЧЕНИЕ
Набор предназначен для количественного определения содержания гемоглобина в крови гемиглобинцианидным методом (метод Drabkin) в клинико-диагностических и биохимических лабораториях.
Набор рассчитан на проведение 600 определений при расходе 5,0 мл рабочего раствора на один анализ.
ПРИНЦИП МЕТОДА
Гемоглобин крови при взаимодействии с железосинеродистым калием (красная кровяная соль) окисляется в метгемоглобин (гемиглобин), образующий с ацетонциангидрином гемиглобинцианид (цианметгемоглобин), интенсивность окраски которого пропорциональна концентрации гемоглобина в крови и измеряется фотометрически при длине волны 540 (500–560) нм.
СОСТАВ НАБОРА
1. Трансформирующий реагент – сухая смесь (натрий углекислый кислый, 1,0 г; калий железосинеродистый, 200 мг) – 3 упаковки.
2. Ацетонциангидрин – 3 ампулы (по 0,5 мл).
3. Калибровочный раствор гемоглобина с концентрацией 120 г/л – 1 флакон (2 мл).
АНАЛИТИЧЕСКИЕ ХАРАКТЕРИСТИКИ НАБОРА
Линейная область определения концентрации гемоглобина – в диапазоне от 20 до 200 г/л, отклонение от линейности – не более 2%.
Чувствительность определения – не более 10 г/л.
Воспроизводимость: коэффициент вариации не более 2%.
Нормальные величины концентрации гемоглобина в крови составляют:
– у мужчин 130–160 г/л;
– у женщин 120–140 г/л.
Качество набора можно оценивать с использованием контрольных растворов гемоглобина отечественного или зарубежного производства.
Рекомендуется в каждой лаборатории уточнить диапазон нормальных величин у обследуемого контингента.
МЕРЫ ПРЕДОСТОРОЖНОСТИ
При работе с данным набором необходимо соблюдать правила техники безопасности, рекомендуемые при работе с кровью в соответствии с Инструкцией по мерам профилактики распространения инфекционных заболеваний при работе в клинико-диагностических лабораториях лечебных и профилактических учреждений, утвержденной Минздравом СССР от 17.01.91 г. и «Правила устройства, техники безопасности, производственной санитарии, противоэпидемического режима и личной гигиены при работе в лабораториях (отделениях, отделах) санитарно-эпидемиологических учреждений системы Министерства здравоохранения СССР».
При работе с набором следует надевать одноразовые резиновые или пластиковые перчатки, так как образцы крови человека следует рассматривать как потенциально инфицированные, способные длительное время сохранять или передавать ВИЧ, вирус гепатита или любой другой возбудитель вирусной инфекции.
В состав трансформирующего раствора входит ацетонциангидрин, ядовитое вещество. В случае попадания раствора на кожу и слизистые необходимо сразу же промыть пораженное место большим количеством проточной воды. Пипетирование per os категорически запрещается. При попадании внутрь следует немедленно выпить 0,5 л теплой воды и вызвать рвоту.
Другие компоненты набора в используемых концентрациях являются нетоксичными.
ОБОРУДОВАНИЕ И РЕАГЕНТЫ
– Спектрофотометр, длина волны 540 нм, или фотоэлектроколориметр, длина волны 500–560 нм (зеленый светофильтр), кювета с толщиной поглощающего свет слоя 10 мм;
– пипетки, позволяющие отбирать объемы жидкости 0,02 и 5,0 мл;
– колба мерная вместимостью 1,0 л;
– пробирки вместимостью 5–10 мл;
– секундомер;
– вода дистиллированная;
– перчатки резиновые или пластиковые.
ПОДГОТОВКА РЕАГЕНТОВ ДЛЯ АНАЛИЗА
Трансформирующий раствор. Один пакет трансформирующего реагента и одну ампулу ацетонциангидрина количественно перенести в мерную колбу вместимостью 1,0 л, растворить в небольшом количестве дистиллированной воды и довести объем дистиллированной водой до метки.
Калибровочный раствор гемоглобина готов к применению.
ПРОВЕДЕНИЕ АНАЛИЗА
В пробирки внести по 5,0 мл трансформирующего раствора, добавить по 0,02 мл крови (разведение в 251 раз), тщательно перемешать и инкубировать при комнатной температуре (+18–25° С) в течение 20 минут, после чего измерить величину оптической плотности опытных проб против холостой пробы (трансформирующего раствора) при длине волны 540 (500–560) нм в кювете с толщиной поглощающего свет слоя 10 мм.
Калибровочный раствор гемоглобина обрабатывать так же, как и пробу цельной крови.
Окраска устойчива в течение 1 часа.
Концентрацию гемоглобина в крови рассчитать по формуле:
Eо
С = --------- х 120 ,
Eк
где: С – концентрация гемоглобина в опытной пробе, г/л;
Eо – оптическая плотность опытной пробы, ед.опт.плотн.;
Eк – оптическая плотность калибровочной пробы, ед.опт.плотн.;
120 – концентрация гемоглобина в калибровочном растворе, г/л.
УСЛОВИЯ ХРАНЕНИЯ И ЭКСПЛУАТАЦИИ НАБОРА
Набор должен храниться в упаковке предприятия-изготовителя при температуре +2–8° С в течение всего срока годности. Допускается хранение наборов при температуре до +25° С не более 5 суток.
Срок годности набора – 2 года.
Трансформирующий раствор должен быть прозрачным, желтого цвета и может храниться в посуде из темного стекла при комнатной температуре не более 6 месяцев. При появлении осадка или при обесцвечивании раствор непригоден для употребления. Не замораживать!
Калибровочный раствор гемоглобина после вскрытия флакона может храниться в течение 6 месяцев, но не более срока годности набора, при хранении в укупоренном виде при температуре +2–8° С.
2.3.1Унифицированный метод определения количества гемоглобина на гемоглобинометре фотометрическом портативном МиниГЕМ
Принцип метода: Основан на превращении гемоглобина в цианметгемоглобин при добавлении к крови реактива (р-р Драбкина). Под влиянием железисто - синеродистого калия гемоглобин окисляется до метгемоглобина (гемоглобина), который затем превращается при помощи калия в цианметгемоглобин (гемоглобинцианид).
Реактивы: 1) Трансформирующий р-р
Устройство: Гемоглобинометр МиниГЕМ 540 представляет собой специализированный фотометр, предназначенный для определения общего гемоглобина крови гемиглобинцианидным методом с фотометрированием на длине волны 540 нм.
Диапазон измеряемой прибором оптической плотности составляет от 0 до 0,9. Б, что соответствует концентрации общего гемоглобина крови от 0 до 360 г/л. В приборе используется стандартная проб подготовка - 20 мкл крови, разведение 1:250. Суммарная погрешность определения гемоглобина (с учетом погрешностей дозаторов и погрешностей биохимического метода), полученная при сравнительных медицинских испытаниях, не превышает 2% (коэффициент вариации) во всем диапазоне измеряемых концентраций. При этом собственная погрешность гемоглобинометра как фотометра - не более 1%, а воспроизводимость, оцененная по коэффициенту вариации, - не более 0,25%.
Два фактора обеспечивают это качество прибора:
высокая воспризводимость характеристик раствора гемиглобинцианида, который сохраняет свои свойства при надлежащем хранении долгие годы, в т. ч. коэффициента пересчета оптической плотности в концентрацию гемоглобина (или фактора калибровки);
конструкция гемоглобинометра МиниГЕМ 540 обеспечивает высокую надежность фотометрических параметров прибора. МиниГЕМ 540 снабжен функцией саморегулирования, он обладает многолетней стабильностью измерений.
Другая отличительная особенность гемоглобинометра - полностью автоматизированная процедура фотометрирования.
Для определения гемоглобина достаточно опустить кювету с фотометрической пробой в прибор, и через мгновенье на дисплее отобразится значение концентрации. Пересчет оптической плотности раствора в концентрацию производится автоматически. Перед измерением прибор не нужно включать, "прогревать", подстраивать или калибровать. Гемоглобинометр автоматически выключится при вынимании кюветы до следующего измерения.
Третья особенность гемоглобинометра МиниГЕМ 540 - его портативность и низкое энергопотребление.
Масса прибора без батарей не превышает 300 г. Питание от сети через адаптер или от встроенных батарей. Ресурс батарей - 1 000 000 измерений, или 4 года работы.
Для контроля работоспособности гемоглобинометра используется контрольная стеклянная мера, паспортизованная для каждого прибора. Внутрилабораторный и внешний контроль качества может проводиться с помощью обычных контрольных материалов -контрольных растворов гемоглобина.
подготовить пробирки, поместив в каждую из них по 5 мл трансформирующего раствора (раствор Драбкина);
во время взятия крови в каждую пробирку перенести по 20 мкл капиллярной крови( 0,02 мл пипеткой Сали) и тщательно перемешать раствор;
через 20 мин каждую пробирку перед измерением перемешать путем переворачивания пробирки вверх вниз (время лизирования) и провести серию измерений:
перелить в оптическую кювету реакционную смесь из очередной пробирки;
опустить оптическую кювету в фотометрическую ячейку прибора, при этом автоматически произойдет фотометрирование реакционной смеси, сопровождаемое звуковым сигналом, и на индикаторе появится число, соответствующее концентрации гемоглобина;
записать результат измерения.
2.3.2 Унифицированный методопределения концентрации гемоглобина на мини -фотометре MF-1020
Введение: мини фотометры являются миниатюрными настольными приборами для измерения гемоглобина крови.
Особенности прибора: цифровой индикатор, кювета открытого типа, относительная устойчивость к светорассеиванию, двухканальная оптическая схема.
Прибор показывает концентрацию гемоглобина в г/л. Светопоглощение зеленого света с длиной волны(546 нм) раствором гемиглобинцианида напрямую переводятся в единицы измерения гемоглобина. Настройка и калибровка прибора осуществляется при помощи двух ручек - « ZERO» и «CAL». К прибору прилагается светофильтр (калибратор), назначение которого - убедиться в исправности оптических и электронных узлов и калибровки минифотометра.
Масса прибора 1 кг 300 гр.
2.В течение 10 мин прогрейте.
3.Убедитесь в том, что прибор правильно откалиброван.
4.Установите кювету с холостой пробой реагента трансформирующего раствора. 5.С помощью ручки « ZERO» на цифровом индикаторе установите нулевое значение. 6.Приготовьте кровь, разбавив ее 1:251 с трансформирующим раствором и проведите измерение.
1 .Двадцать микрометров крови (0,02 мл) необходимо разбавить в 5 ,0 мл трансформирующего раствора р-ра Драбкина- 1:21
2.Хорошо перемешайте (встряхните). Прежде чем приступить к измерению, подождите 5-10 мин, особенно если реагент не содержит детергент.
Калибровка минифотометра по стандартному р-ру гемиглобинцианида
Вставьте кювету, содержащую трансформирующий реактив (р-р Драбкина) в кюветный отсек.
При помощи ручки « ZERO» установите нулевое значение в цифровом табло.
Вставьте кювету, содержащую стандартный р-р гемиглобинцианида, в кюветный отсек.
При помощи ручки « CAL» установите данное значение стандартного калибровочного р-ра в цифровом табло (пример 150 г/л).
Повторите процедуру калибровки от пункта 1 до пункта 4.
Калибровка окончена, и Вы можете приступить к измерению
Калибровка минифотометра при помощи калибратора (по фактору)
1.Вставьте калибратор со светофильтром в кюветный отсек таким образом, чтобы была
видна надпись «ZERO» с цифровым значением (например, 0.1.6)
2.При помощи ручки «ZERO» установите это значение (п.п.0.1.6) в цифровом табло.
3.Переверните калибратор и вставьте его в кюветный отсек таким образом, чтобы
была видна надпись «CAL» с калибровочным значением (пример 159).
4.При помощи ручки «CAL» установите данное значение на цифровом табло.
Повторите процедуру от пункта 1 до пункта 4.
Калибровка окончена, и Вы можете приступать к измерениям.
Требования к реактивам:
1.Любая модификация р-ра пригодна для применения.
2.Разбавление 10 мкл крови в 2,5 мл трансформирующего не пригодно для этой модели.
3.Можно приготавливать самим р-р-1 раз в месяц, хранится в посуде из темного стекла.
2.3.3 Унифицированный метод определения гемоглобина на фотоэлектроколориметре
Принцип метода: Гемоглобин, взаимодействуя с ацетонциангидрином, в присутствии железосинеродистого калия K3 [Fe(CN)6 ] образует гемиглобинцианид красного цвета, интенсивность окраски которого пропорциональна содержанию гемоглобина в пробе крови.
Реактивы: 1) трансформирующий раствор (0,5 мл ацетонциангидрина, 0,2 г железосинеродистого калия, 1 г гидрокарбоната натрия NaHCb растворяют в 1 л дистиллированной воды; реактив стоек, хранится в посуде из темного стекла); 2) стандартный раствор гемиглобинцианида (раствор, выпускаемый фирмой «Ренал», содержит 59,75 мг% гемиглобинцианида; раствор фирмы «Иммуна» —64,23 мг%. Это соответствует концентрации гемоглобина в крови 150 и 154 г/л при разведении ее в 251 раз).
Ход определения. К 5мл трансформирующего раствора добавляют 0,02 мл (капилляр Сали) крови. При этом кровь разводится в 251 раз. Оставляют пробирки на 20 мин при комнатной температуре.
Фотометрируют при зеленом светофильтре (длина волны 540 нм) в кювете с толщиной слоя 10 мм (1 см) против дистиллированной воды.
Стандартный раствор фотометрируют при тех же условиях, что и опытную пробу.
Расчет. Содержание гемоглобина определяют по калибровочному графику, который строится по стандартному раствору гемиглобинцианида или по формуле:
Где С- концентрация гемоглобина в опытной пробе, г/л
Ео - оптическая плотность опытной, ед. опт. Плотность
Ек- оптическая плотность калибровочной пробы, ед.плот.
120-концекнтрация гемоглобина кВ калибровочном растворе, г/л.
Приготовленные разведения фотометрируют. против дистиллированной воды («холостая» проба).
Eк – оптическая плотность калибровочной пробы, ед.опт.плотн.;
120 – концентрация гемоглобина в калибровочном растворе, г/л.
УСЛОВИЯ ХРАНЕНИЯ И ЭКСПЛУАТАЦИИ НАБОРА
Набор должен храниться в упаковке предприятия-изготовителя при температуре +2–8° С в течение всего срока годности. Допускается хранение наборов при температуре до +25° С не более 5 суток.
Срок годности набора – 2 года.
Трансформирующий раствор должен быть прозрачным, желтого цвета и может храниться в посуде из темного стекла при комнатной температуре не более 6 месяцев. При появлении осадка или при обесцвечивании раствор непригоден для употребления. Не замораживать!
Калибровочный раствор гемоглобина после вскрытия флакона может храниться в течение 6 месяцев, но не более срока годности набора, при хранении в укупоренном виде при температуре +2–8° С.
По вопросам, касающимся приобретения наборов и их качества, просим обращаться по адресу: 105173, г. Москва, ул. Западная, д. 2, стр. 1, ООО «Агат–Мед». Телефон для справок (495) 777-41-92.
Инструкция составлена: к.б.н. И.В. Смирновым – ст.н.с. Гематологического научного центра РАМН, к.б.н. Н.Н. Контугановым, В.В. Майоровой – сотрудниками ООО «Агат–Мед».





• масло иммерсионное
классическое Агат-Мед
• масло иммерсионное
профессиональное Агат-Мед
• масло иммерсионное
Минимед
+ Красители
и химические реактивы
• красители по Романовскому
по Май-Грюнвальду ,
по Лейшману
• калий теллурит водный,
раствор 2%
• набор реактивов
Азопирамовой пробы для
контроля качесва очистки
изделий мед. назначения

НАЗНАЧЕНИЕ
Набор предназначен для количественного определения содержания гемоглобина в крови гемиглобинцианидным методом (метод Drabkin) в клинико-диагностических и биохимических лабораториях.
Набор рассчитан на проведение 600 определений при расходе 5,0 мл рабочего раствора на один анализ.
ПРИНЦИП МЕТОДА
Гемоглобин крови при взаимодействии с железосинеродистым калием (красная кровяная соль) окисляется в метгемоглобин (гемиглобин), образующий с ацетонциангидрином гемиглобинцианид (цианметгемоглобин), интенсивность окраски которого пропорциональна концентрации гемоглобина в крови и измеряется фотометрически при длине волны 540 (500–560) нм.
СОСТАВ НАБОРА
1. Трансформирующий реагент – сухая смесь (натрий углекислый кислый, 1,0 г; калий железосинеродистый, 200 мг) – 3 упаковки.
2. Калибровочный раствор гемоглобина с концентрацией 120 г/л – 1 флакон (2 мл).
АНАЛИТИЧЕСКИЕ ХАРАКТЕРИСТИКИ НАБОРА
Линейная область определения концентрации гемоглобина – в диапазоне от 20 до 200 г/л, отклонение от линейности – не более 2%.
Чувствительность определения – не более 10 г/л.
Воспроизводимость: коэффициент вариации не более 2%.
Нормальные величины концентрации гемоглобина в крови составляют:
– у мужчин 130–160 г/л;
– у женщин 120–140 г/л.
Качество набора можно оценивать с использованием контрольных растворов гемоглобина отечественного или зарубежного производства.
Рекомендуется в каждой лаборатории уточнить диапазон нормальных величин у обследуемого контингента.
ОБОРУДОВАНИЕ И РЕАГЕНТЫ
– Спектрофотометр, длина волны 540 нм, или фотоэлектроколориметр, длина волны 500–560 нм (зеленый светофильтр), кювета с толщиной поглощающего свет слоя 10 мм;
– пипетки, позволяющие отбирать объемы жидкости 0,02 и 5,0 мл;
– колба мерная вместимостью 1,0 л;
– пробирки вместимостью 5–10 мл;
– секундомер;
– вода дистиллированная;
– перчатки резиновые или пластиковые.
ПОДГОТОВКА РЕАГЕНТОВ ДЛЯ АНАЛИЗА
Трансформирующий раствор. Один пакет трансформирующего реагента и одну ампулу ацетонциангидрина количественно перенести в мерную колбу вместимостью 1,0 л, растворить в небольшом количестве дистиллированной воды и довести объем дистиллированной водой до метки.
Калибровочный раствор гемоглобина готов к применению.
ПРОВЕДЕНИЕ АНАЛИЗА
В пробирки внести по 5,0 мл трансформирующего раствора, добавить по 0,02 мл крови (разведение в 251 раз), тщательно перемешать и инкубировать при комнатной температуре (+18–25° С) в течение 20 минут, после чего измерить величину оптической плотности опытных проб против холостой пробы (трансформирующего раствора) при длине волны 540 (500–560) нм в кювете с толщиной поглощающего свет слоя 10 мм.
Калибровочный раствор гемоглобина обрабатывать так же, как и пробу цельной крови.
Окраска устойчива в течение 1 часа.
Концентрацию гемоглобина в крови рассчитать по формуле:
где: С – концентрация гемоглобина в опытной пробе, г/л;
Eо – оптическая плотность опытной пробы, ед.опт.плотн.;
Eк – оптическая плотность калибровочной пробы, ед.опт.плотн.;
120 – концентрация гемоглобина в калибровочном растворе, г/л.
УСЛОВИЯ ХРАНЕНИЯ И ЭКСПЛУАТАЦИИ НАБОРА
Набор должен храниться в упаковке предприятия-изготовителя при температуре +2–8° С в течение всего срока годности. Допускается хранение наборов при температуре до +25° С не более 5 суток.
Срок годности набора – 2 года.
Трансформирующий раствор должен быть прозрачным, желтого цвета и может храниться в посуде из темного стекла при комнатной температуре не более 6 месяцев. При появлении осадка или при обесцвечивании раствор непригоден для употребления. Не замораживать!
Калибровочный раствор гемоглобина после вскрытия флакона может храниться в течение 6 месяцев, но не более срока годности набора, при хранении в укупоренном виде при температуре +2–8° С.
Определение гемоглобина является одним из важнейших и основных лабораторных исследований. Наряду с подсчетом эритроцитов, это важнейший лабораторный показатель для оценки анемических состояний.
Гемоглобин — основной дыхательный белок крови, относящийся к хромопротеидам. Состоит из белковой (глобин) и небелковой (гем) части. Он является белком четвертичной структуры и состоит из четырех субъединиц, каждая из которых включает полипептидную цепь, соединенную с гемом. Полипептидные цепи попарно одинаковы: 2 цепи глобина типа ? и 2 цепи глобина другого типа (?, ? и ?), соединенные с 4 молекулами гема.
Гем — это молекула протопорфирина ІХ, связанная с атомом железа. Каждый тетрамер гемоглобина может обратимо связывать и транспортировать не более 4-х молекул кислорода. 65 % гемоглобина образуется в эритроците в ядросодержащих стадиях созревания, 35 % — в стадию ретикулоцита. В стадии зрелого нормоцита синтез гемоглобина прекращается.
В настоящее время известно 3 главных подтипа гемоглобина: Hb А, Hb F и Hb А2. Основным является подтип А, который в норме составляет 96–98 % общего гемоглобина, тогда как Hb А2 составляет всего 23 %. Фетальный гемоглобин, преобладающий в крови новорожденного (Hb F), присутствует в крови у взрослого человека в количестве 1–1,5 %.
Кроме нормальных типов гемоглобина в настоящее время выделено еще около 20 его патологических вариантов. Как нормальные, так и патологические типы гемоглобина различаются не по структуре порфиринового кольца, а по строению глобина.

Существуют три основные группы методов определения количества гемоглобина:
Ранее широко применялся колориметрический гематиновый метод, известный под названием метода Сали, который весьма несложен и удобен, но очень неточен.
В настоящее время используются главным образом циангемоглобиновые методы, в которых лучше всего сочетаются точность и техническая простота.
Газометрические методы и методы, основанные на определении железа точны, но требуют много времени и поэтому не нашли широкого практического применения.
Читайте также: Определение количества гемоглобина Определение количества гемоглобина в крови циангемоглобиновым методомУнифицированный метод определения гемоглобина, наиболее широко применяемый в клинических лабораториях Украины.
1. Принцип метода.Гемоглобин при взаимодействии с железосинеродистым калием окисляется в метгемоглобин, образующий с ацетонциангидрином окрашенный гемоглобинцианид, интенсивность окраски которого пропорциональна содержанию гемоглобина.
2. Реактивы:а) трансформирующий раствор, содержащий ацетонциангидрин (0,5 мл), калий железосинеродистый (200 мг), бикарбонат натрия (1 г), дистиллированную воду (до 1000 мл). При появлении мути раствор не пригоден к употреблению;
б) стандартный раствор гемоглобинцианида — 5 мл. Концентрация гемоглобинцианида — 150 г/л.
В мерную колбу на 1000 мл внести приблизительно 500 мл дистиллированной воды, количественно прибавить содержимое флакона смеси реактивов и содержимое 1 ампулы ацетонциангидрина, перемешать и дополнить дистиллированной водой до метки, перемешать и перелить в посуду для хранения. Хранить в прохладном, темном месте.
4. Ход определения20 мкл крови прибавляют к 5 мл трансформирующего раствора, хорошо перемешивают, оставляют стоять 20 мин, после чего измеряют на фотоэлектроколориметре при длине волны 500–560 нм (зеленый светофильтр) в кювете с толщиной слоя 1 см против трансформирующего раствора или дистиллированной воды. Стандартный раствор колориметрируют без обработки.
5. Расчет где 150 — концентрация гемоглобинцианида;
где 150 — концентрация гемоглобинцианида;
Ест — экстинкция стандартного раствора;
Епр — экстинкция пробы.
Результат выражается в г/л.
Для ориентировочного определения гемоглобина крови иногда используют гемометр Сали (рис. 1)*. Метод основан на сравнении интенсивности окраски исследуемого раствора с интенсивностью окраски стандартного раствора. Гемоглобин крови под действием соляной кислоты превращается в солянокислый гематин, окрашивающий раствор в коричневый цвет.
Полученный раствор колориметрируют:
Данный метод является устаревшим, субъективным, требует регулярной проверки окраски стандартной шкалы и в настоящее время применяется редко.
Другие методы определения количества гемоглобинаНа современном уровне развития методов диагностики совершенно недостаточно ограничиваться определением общего количества гемоглобина, так как в некоторых случаях определение качественного состава имеет решающее диагностическое значение.
Гемоглобин циркулирует в крови в форме нескольких производных.
Присоединение кислорода (к железу гема) приводит к образованию оксигемоглобина (HbO2 ). Отдав кислород тканям, оксигемоглобин превращается в восстановленную форму (HbO2 - НHb).
Удаление углекислого газа из тканей происходит путем его присоединения к свободным аминным группам глобина и при этом образуется карбаминогемоглобин (карбгемоглобин).
Окись углерода (СО) присоединяется к железу гема, в результате чего образуется стойкое соединение карбоксигемоглобин. Окись углерода является продуктом обмена и образуется эндогенно при распаде гема (в норме при старении эритроцитов).
Содержание карбоксигемоглобина, в первую очередь, является показателем гемолиза. Железо гема находится в двухвалентной форме. При окислении его (Fe++ - Fe+++) образуется метгемоглобин. Окислителями железа гема могут быть различные продукты метаболизма — активные формы кислорода, ферменты, альдегиды и др. В норме за сутки образуется 2,5% метгемоглобина, а обнаруживается в крови 1,5%. Метгемоглобинредуктазная система восстанавливает метгемоглобин, переводя его в восстановленную форму, возвращая тем самым способность транспортировать кислород.
К экзогенным метгемоглобинобразователям относятся нитриты, нитраты, присутствующие в избыточном количестве в воде, в пище, ряд лекарственных препаратов.
Гемоглобин, соединяясь с различными сульфопроизводными в комплексы, образует сульфметгемоглобин. У здоровых людей это производное гемоглобина не содержится в крови. Обнаружение его свидетельствует о повышенном содержании сульфопроизводных в воде, пище, воздухе. В связи с этим сульфметгемоглобин является маркером экологической обстановки.
Диагностическое значение имеет определение гликозилированных гемоглобинов, образующихся в результате комплексирования гемоглобина с различными углеводородами. 95 % от общего количества гликозилированных гемоглобинов приходится на долю гемоглобина А1с, образующегося в результате комплексирования гемоглобина и глюкозы. Дифференциацию производных гемоглобина проводят спектроскопически.
Типы гемоглобина имеют большое значение не только для диагноза, но и перемещают вопрос о патогенезе анемии из чисто морфологической области в биохимическую.
Анемии, вызываемые появлением патологического типа гемоглобина, называются гемоглобинопатиями. К настоящему времени открыто более 600 аномальных гемоглобинов. Известны гемоглобинопатии М, С, Д, «Волга», «Хельсинки» и др. Они могут быть качественными и количественными. Качественные возникают в результате замены аминокислот. Количественные гемоглобинопатии обусловлены изменением скорости синтеза полипептидных цепей.
Количественное содержание гемоглобинау новорожденного — 136–196 г/л;
у трехмесячного — 105–125 г/л;
у ребенка в возрасте 1 года — 110–130 г/л;
у ребенка в возрасте 10 лет — 115–148 г/л;
у взрослого мужчины — 130–160 г/л;
у взрослой женщины — 120–140 г/л.
Пониженная концентрация гемоглобина в крови называется олигохромемией (или гемоглобинопенией). Наблюдается при:
Гиперхромемия — редкое явление и не имеет большого клинического значения. Она встречается при:
На современном уровне развития методов диагностики совершенно недостаточно ограничиваться определением общего количества гемоглобина, так как в некоторых случаях определение качественного состава имеет решающее диагностическое значение.
Гемоглобин циркулирует в крови в форме нескольких производных. Присоединение кислорода (к железу гема) приводит к образованию оксигемоглобина (HbО2). Отдав кислород тканям, оксигемоглобин превращается в восстановленную форму (HbО2 - НHb).
Удаление углекислого газа из тканей происходит путем его присоединения к свободным аминным группам глобина и при этом образуется карбаминогемоглобин (карбгемоглобин). Окись углерода (СО) присоединяется к железу гема, в результате чего образуется стойкое соединение карбоксигемоглобин. Окись углерода является продуктом обмена и образуется эндогенно при распаде гема (в норме при старении эритроцитов). Содержание карбоксигемоглобина, в первую очередь, является показателем гемолиза.
Железо гема находится в двухвалентной форме. При окислении его (Fe++ - Fe+++) образуется метгемоглобин. Окислителями железа гема могут быть различные продукты метаболизма — активные формы кислорода, ферменты, альдегиды и др. В норме за сутки образуется 2,5 % метгемоглобина, а обнаруживается в крови 1,5 %.
Метгемоглобинредуктазная система восстанавливает метгемоглобин, переводя его в восстановленную форму, возвращая тем самым способность транспортировать кислород. К экзогенным метгемоглобинобразователям относятся нитриты, нитраты, присутствующие в избыточном количестве в воде, в пище, ряд лекарственных препаратов.
Гемоглобин, соединяясь с различными сульфопроизводными в комплексы, образует сульфметгемоглобин. У здоровых людей это производное гемоглобина не содержится в крови. Обнаружение его свидетельствует о повышенном содержании сульфопроизводных в воде, пище, воздухе. В связи с этим сульфметгемоглобин является маркером экологической обстановки.
Диагностическое значение имеет определение гликозилированных гемоглобинов. образующихся в результате комплексирования гемоглобина с различными углеводородами. 95 % от общего количества гликозилированных гемоглобинов приходится на долю гемоглобина А1с, образующегося в результате комплексирования гемоглобина и глюкозы. Дифференциацию производных гемоглобина проводят спект роскопически.
Типы гемоглобина имеют большое значение не только для диагноза, но и перемещают вопрос о патогенезе анемии из чисто морфологической области в биохимическую.
Анемии, вызываемые появлением патологического типа гемоглобина, называются гемоглобинопатиями. К настоящему времени открыто более 600 аномальных гемоглобинов. Известны гемоглобинопатии М, С, Д, «Волга», «Хельсинки» и др. Они могут быть качественными и количественными. Качественные возникают в результате замены аминокислот. Количественные гемоглобинопатии обусловлены изме- нением скорости синтеза полипептидных цепей.
Читайте также:Оценка полученных данных. В норме концентрация в крови гемогло бина составляет у женщин 120-140 г/л (12-14 г%), у мужчин — 130-160 г/л
Определение гемоглобина унифицированным гемоглобинцианидным методом
Принцип метода: гемоглобин окисляют железосинеродистым калием (красная кровяная соль) в метгемоглобин (гемиглобин). Образующийся при взаимодействии гемиглобина с ацетонциангидрином окрашенный гемоглобин-цианид определяют фотометрически. Его интенсивность пропорциональна со держанию гемоглобина.
Оборудование и реактивы:
1. Смесь реактивов для приготовления трансформирующего раствора: калий железосинеродистый (красная кровяная соль) — 200 мг; натрия бикарбонат — 1 г; ацетонциангидрин — 0,5 мл; дистиллированная вода — до 1 л.
2. Стандарт гемоглобина (лиофилизат).
3. Фотоэлектрокалориметр, спектрофотометр или гемоглобинометр.
4. Пипетка на 0,02 мл.
5. Колба мерная на 1,0 л.
Приготовление трансформирующего раствора: смесь реактивов и ацетонциангидрин количественно перенести в мерную колбу емкостью 1 л, довести до метки дистиллированной водой и перемешать.
Приготовление стандартного раствора: вскрыть флаконы с лиофилизатом гемоглобина. Растворить содержимое флакона в 5 мл трансформирующего рас
твора и перемешать, избегая вспенивания. Хранить стандартный раствор при 2-8°С.
Методика: 0,02 мл крови (капилляр Сали) приливают к 5 мл трансформирующего раствора (разведение в 251 раз) и перемешивают. Через 10 мин на фотоэлектроколориметре измеряют оптическую плотность при длине волны 500-560 нм (зеленый светофильтр) относительно «холостой» пробы (трансфор мирующий раствор). Для определения концентрации гемоглобина при этих же условиях измеряют оптическую плотность стандартного раствора.
Рассчитывают концентрацию гемоглобина (НЬ) (г/л) по калибровочному графику, построенному по стандартному раствору гемоглобинцианида или по формуле:
НЬ = (А пробы / А стд) х С стд х К х 0,01,
где А пробы — оптическая плотность опытной пробы; А стд — оптическая плотность стандартного раствора; С стд — концентрация гемоглобинцианида в стандартном растворе; К — коэффициент разведения крови; 0,01 — коэффици ент пересчета мг% в г/л.
Измеряют против «холостой» пробы на спектрофотометре при длине волны 540 нм или на гемоглобинометре.
Пределы колебаний концентрации гемоглобина у здоровых людей: у мужчин — 130-160 г/л, у женщин — 120-140 г/л.